ǰ���о����֣�T-ZnOw�����������õĿ������������ұ��ֳ����õķֽ��ȩ���к��л����Ч����Ϊ�˿�������Թ��ɼ����̣��������л�Ⱦ�Ϸ�ˮ֮һ�ļ���Ϊ��������о���T-ZnOw�ֽ��л���ķ�Ӧ����ѧ�������˴���Ũ�ȡ����ȳ�ʼŨ�ȵ����ض�����Ч����Ӱ�죬������ͨ��������TiO2�Ĺ�������������˱Ƚϡ�
2 ���鲿��
2.1 ʵ��ԭ��
T-ZnOw�볤Ϊ30��50��m�����Ϊ�����ߴ磬��ò��ͼ1�����ѿ�ṹ������TiO2Ϊ��ͨ���νṹ������Ϊ20��30���ס�
2.2 ʵ��װ�ü�����
�����Ӧװ���ڴ���������ϣ���40W����ƴ�ֱ���䣬��Դ��Һ��260mm���������Ӧװ�÷�����һ���������С�
ʵ��ʱ������ȡ��һ�����Ĵ�������������õ�500ml������Һ��PHֵΪ6���У����ڴ���������Ͻ���30min��ʹ��������ȷ��ӳ�ֽӴ���Ȼ������������䡣��ʵ������У���ʱ��һ������ӦҺ�����Ļ����ĺ�ȡ�ϲ���Һ���зֹ��ȼ�⡣
2.3 �������
��Ʒ�����UV-550�����⣭�ɼ��ֹ��ȼ��Ͻ��С����ȶ�ʵ��Ũ�ȵļ�����Һ����ȫ��ɨ�裬ȷ�����ȵ�������ղ���Ϊ461nm����ͼ2��ʾ��Ȼ����������ղ������ⶨ����Ʒ������ȡ����ü��ȵ���ɫЧ�������������Ĺ����������ɫ��ʣ������������ʾ��
���������� ��100�� ��1��
���У�����ʾɫ��ʣ���ʣ�Ai��ʾ��Ӧijһʱ�̵�����ȣ�A0��ʾ��ʼ����ȡ�

Fig.2 UV-Vis Spectrum of Methyl Orange Solution (10mg/L)
3 ���������
3.1 T-ZnOw������ⷴӦ����ѧ�����о�
Ŀǰ���뵼 ����Ϲ�����ⷴӦ�Ķ���ѧģ����Ҫ������[6]��һ����Langmuir �CHinshelwood��L-H��ģ�ͣ���һ����Eley-Rideal��E-R��ģ�͡�ǰ����Ϊ�л������������������棬Ȼ����һ�������Ӧ����������Ϊ�л������Һ���������������Բ�λ��ɢ�����������Ӧ��
Ϊ���о�T-ZnOw���������ȵķ�Ӧ����ѧ���ɣ���ʵ����40W������������£�����T-ZnOw��Ũ��Ϊ2g/L�����10mg/L��20mg/L��30mg/L�ļ�����Һ������ʵ�顣ʵ�����õ����ݾ��������Ժ�����ͼ3��ʾ��
��ͼ�����ǿ��Կ�����-ln �� �뷴Ӧʱ��t֮���нϺõ����Թ�ϵ������������Һ��ʼŨ�ȵĽ��ͣ�ֱ�ߵ�б����������������Ͻ�����֣�����ɻ�������һ������ѧ����
-ln (Ai/A0)��kt ��2��
����L-Hģ����������ۡ�����������Һ��ʼŨ�ȵ����ӣ���Ӧ���ʳ���k���ν��͡��������ݼ������������10mg/L��20mg/L��30mg/L�ļ�����Һ��T-ZnOw���������Һ�ķ�Ӧ���ʳ����ֱ�Ϊ0.21216��0.04875��0.03925 (h-1)��
����L-Hģ�����ۣ���������������л��������������ı��棬������ҺŨ�ȵ����ӣ�Խ��Խ��ļ��ȷ��Ӿۼ���T-ZnOw���棬�����ڱ�����⼤�������ڼ���̬�ļ��ȷ��ӻ���֮�����ûᵼ�´���[7]�����ִ����ʻ�������ҺŨ�ȵ����Ӷ��������ԣ�����ʹ���ֳ����ķ�Ӧ������Ӧ���͡�
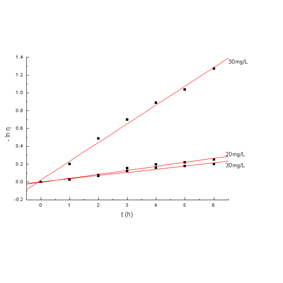
Fig.3 Relationship Between �Cln��and t 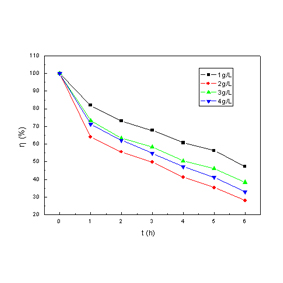
Fig. 4 Effects of Dosage of the Catalys
t3.2 ����Ũ�ȶԹ������Ч����Ӱ��
�ӹ����ԭ����֪����������Ч����Ҫȡ���ڴ�����һ�������²����Ĺ������ӵ�Ũ�ȡ����ԣ��ڷ�Ӧ�����У�����Ũ��ֱ��Ӱ���Ź����Ч����Ϊ�˷������������Է�Ӧ��Ӱ�죬��ʵ����T-ZnOwΪ�������̶��˼��ȵ�Ũ��Ϊ10mg/L��PHֵΪ6���ң���40W����Ƶ�ֱ�������½��С�ʵ��֤����������û�м�������������·�Ӧ6��Сʱ�������û�з����κα仯����������Ũ�ȷֱ�Ϊ1g/L��2 g/L��3 g/L��4 g/Lʱ���併��Ч����ͼ4��ʾ��
���Կ�������T-ZnOwŨ��Ϊ2g/Lʱ�Ĵ�Ч��Ҫ������������Ũ��ʱ�Ĵ�Ч����������Ϊ������Ҫ������ڷ�Ӧ�в����Ļ���������������Һ�еĹ�ѧ�����йء�������Ũ��ƫ��ʱ����Ӧ�в����Ļ�������Ũ����Ӧ�ϵͣ�������Ч���ϲ��֮����������ʽ�������ɢ��ǿ���뵥λ����������������ȣ���֪������Һ�д���Ũ�ȹ���ʱ����Ӧ��������ɢ��Ҳ��Խǿ�ң���������ʽ��ͣ���Ӧ�Ĵ�����Ч��Ҳ�ή�͡�ֻ�дﵽ�����ߵ�ƽ��ʱ�����ܲ�����õĴ�Ч�����ڱ�ʵ���У�T-ZnOw�����Ũ��Ϊ2g/L��
3.3����Ũ�ȶԹ������Ч����Ӱ��
���ȳ�ʼŨ�ȶԹ��������һ����Ӱ�졣�ڱ�ʵ���У������̶�T-ZnOw��Ũ��Ϊ2g/L���ı������Һ�ij�ʼŨ�ȣ��ֱ�Ϊ10mg/L��15 mg/L��20 mg/L��25 mg/L��30 mg/L������ͬ�ķ�Ӧ�����£��õ����ǵ�ɫ��ʣ���ʱ仯���ߣ���ͼ5��ʾ��
���Կ�������Ӧ��������Һ���յ�ɫ��ʣ�������ż��ȳ�ʼŨ�ȵ����Ӷ����T-ZnOw�����ﵽ���ͻ����ʱ������T-ZnOw�����������Ľ��ܵ�Ӱ�졣��һ���棬������Һ��ɫ������Ҳ����һ���������ԣ���ҺŨ��Խ�ߣ���ɫԽ���Ӧ��������Ҳ��Խ�ã������õ������ǿ����Լ�����

Fig.5 Effect of the Initial Concentration

Fig.6 Comparison Effect of T-ZnOw and TiO2
3.4 ��������Թ������Ч����Ӱ��
�뵼����ϵĹ�����������ܶ������йأ���������������������ࡢŨ���Լ������������ȣ�������������ϵ��������������ò�йء�
Ŀǰ�ձ��о��ľ��й�����ԵIJ���Ϊ��ͨ��������ZnO������TiO2���ֹ�����ϣ������ھ���������ò��T-ZnOw���������ܵĶԱ��о������١��о��ձ���Ϊ����TiO2���������Ҫ��������ZnO��Ϊ�ˣ����Ķ�����TiO2��T-ZnOw�����ֲ�ͬ������Ͻ����˶Ա��о������ͼ6��ʾ��
ʵ�鷢�֣��ڱ�ʵ��ķ�Ӧ��������T-ZnOw�Ĺ������Ч��Ҫ������������TiO2���ӹ�������ԭ���������������Ƚ��л������������棬������������������������������ԾǨ�γ����ɵ��ӺͿ�Ѩ�����ɵ�����ˮ�е�����ˮͨ��һϵ�еķ�Ӧ����������ǿ�����Ե��ǻ����ɻ����ǻ����ɻ���ʹ������л������ս���Ϊ������̼��ˮ���ɴ˿��Կ��������Ч����Ҫȡ���ڴ����������ӵ�Ũ�ȡ��Ӷ����Գ�������T-ZnOw�����Ч�����ŵ�ԭ��������T-ZnOw���������״�ṹ�������ž۵Ŀ��ܣ�����������ļ��ȷ��ӣ���Σ�����T-ZnOw��������ò������״��ṹ�Ӹ�������ˣ��ߴ���С�������ڸýṹ�д���ϵ���ܼ��������ڲ����ĵ��ӺͿ�϶���룻���ߣ����е����ṹ��T-ZnOw������û�о��磬�����ڹ�̼����������ɵ��ӻ��϶��ͳ�ƻ������ģ����ٴ��䵽�������棬�Ӷ����ֳ���Ч�����ԡ�
4 �� ��
��1��T-ZnOw�Լ�����Һ�������õĽ���Ч�����䷴Ӧ����һ������ѧ���ɡ�